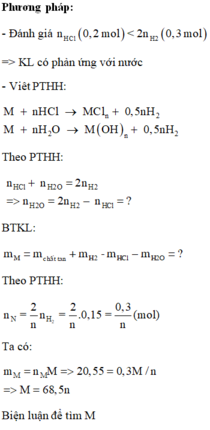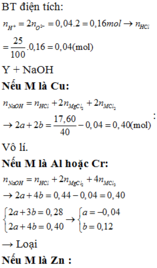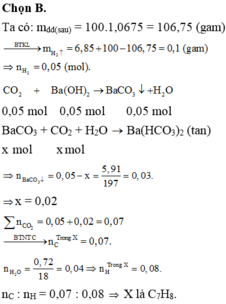Hòa tan 8gam kim loại kiềm M trong 92.4 gam nước sau khi phản ứng xảy ra hoàn toàn thu được dung dịch A có C%=14.8 % Tìm kim loại M

Những câu hỏi liên quan
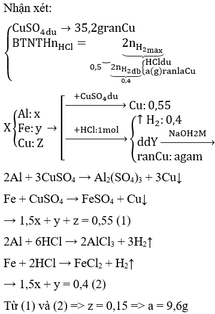
Hỗn hợp X gồm ba kim loại Al, Fe, Cu. Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.Viết phương trình phản ứng xảy ra và tìm giá trị của a.
Đọc tiếp
Hỗn hợp X gồm ba kim loại Al, Fe, Cu. Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.Viết phương trình phản ứng xảy ra và tìm giá trị của a.
Hòa tan kim loại M vào 200 ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí
H
2
(đktc) và dung dịch X chứa 29,35 gam chất tan. Kim loại M là A. Na B. Ba C. K D. Al
Đọc tiếp
Hòa tan kim loại M vào 200 ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí H 2 (đktc) và dung dịch X chứa 29,35 gam chất tan. Kim loại M là
A. Na
B. Ba
C. K
D. Al
1) Xác định tên kim loại A và M khi:a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
Đọc tiếp
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
Đúng 1
Bình luận (0)
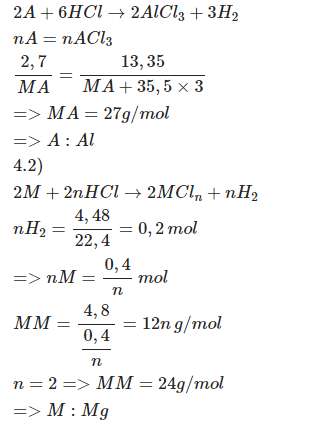
\(\Rightarrow\) \(M:mg\)
đun nóng m gam kim loại M có hóa trị không đổi trong không khí đến khi phản ứng xảy ra hoàn toàn thì thu được oxit có khối lượng 1,25m gam .Để hòa tan hết lượng oxit trên cần 200 g dung dịch H2SO4 19,6% thu được dung dịch X .Xác định kim loại M .Tính nồng độ phần trăm C% của chất tan có trong dung dịch X
Gọi n là hóa trị của M
Phản ứng xảy ra:
4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol
→mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m
→MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Hòa tan oxit
CuO+H2SO4→CuSO4+H2O
Ta có:
mH2SO4=200.19,6%=39,2 gam
→nH2SO4=39,298=0,4 mol = nCuO=nCuSO4
→mCuO=0,4.(64+16)=32 gam;mCuSO4=0,4.(64+96)=64 gam
Áp dụng định luật bảo toàn khối lượng:
mddX=mCuO+mddH2SO4=200+32=232 gam
→C%CuSO4=64232=27,5862%
chúc bạn học tốt
Đúng 0
Bình luận (0)
Gọi n là hóa trị của M Phản ứng xảy ra: 4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol →mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m →MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Đúng 0
Bình luận (0)
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn. a) Xác định công thức muối sunfat của kim loại kiềm ban đầu. b) Tính nồng độ % của các chất tan trong dung dịch A. c) Dung dịch muối sunfat của kim l...
Đọc tiếp
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m < 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức muối sunfat của kim loại kiềm ban đầu.
b) Tính nồng độ % của các chất tan trong dung dịch A.
c) Dung dịch muối sunfat của kim loại kiềm ban đầu có thể tác dụng được với các chất nào sau đây: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Ag, Fe, CuS, Fe(NO3)2? Viết phương trình hóa học của các phản ứng xảy ra.
a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
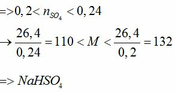
b)
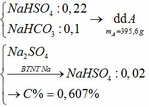
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O
Đúng 0
Bình luận (0)
Cho 2,24 lít (đktc) hỗn hợp gồm
C
l
2
v
à
O
2
tác dụng vừa đủ với 5,82 gam hỗn hợp gồm Mg và kim loại M, thu được 11,36 gam chất rắn X. Hòa tan hết X trong dung dịch HCl (đun nóng, dùng dư 25% so với lượng phản ứng), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thấy có 17,60 gam NaOH phản ứng. Biết các phản ứng xảy ra hoàn toàn, hiđroxit của M ít tan trong nước. Cho bi...
Đọc tiếp
Cho 2,24 lít (đktc) hỗn hợp gồm C l 2 v à O 2 tác dụng vừa đủ với 5,82 gam hỗn hợp gồm Mg và kim loại M, thu được 11,36 gam chất rắn X. Hòa tan hết X trong dung dịch HCl (đun nóng, dùng dư 25% so với lượng phản ứng), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thấy có 17,60 gam NaOH phản ứng. Biết các phản ứng xảy ra hoàn toàn, hiđroxit của M ít tan trong nước. Cho biết M là kim loại nào sau đây
A. Cu
B. Cr
C. Al
D. Zn
:Người ta cho a mol nguyên tử kim loại M tan vừa hết trong dung dịch có chứa a mol phân từ H2SO4 thu được 7,8 gam muối A và thoát ra khí A1 . Hấp thu toàn bộ lượng khí A1 trong 450 ml dung dịch NaOH 0,1M thu được dung dịch A2 có chứa 3,04 g muối . Toàn bộ lượng khí A thu được hòa tan vào nước sau đó thêm 1,935 g hỗn hợp B gồm kẽm và đòng , sau khi thấy phản ứng xảy ra hoàn toàn thu được 5,72 g chất rắn C gồm hai kim loại . a) tính M và tính a b) Tính khối lượng của kim loại trong hỗn hợp B và ch...
Đọc tiếp
:Người ta cho a mol nguyên tử kim loại M tan vừa hết trong dung dịch có chứa a mol phân từ H2SO4 thu được 7,8 gam muối A và thoát ra khí A1 . Hấp thu toàn bộ lượng khí A1 trong 450 ml dung dịch NaOH 0,1M thu được dung dịch A2 có chứa 3,04 g muối . Toàn bộ lượng khí A thu được hòa tan vào nước sau đó thêm 1,935 g hỗn hợp B gồm kẽm và đòng , sau khi thấy phản ứng xảy ra hoàn toàn thu được 5,72 g chất rắn C gồm hai kim loại . a) tính M và tính a b) Tính khối lượng của kim loại trong hỗn hợp B và chất rắn C
tội nghiệp cô bé đăng 5 năm ko có ai trả lời
Đúng 0
Bình luận (0)
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là A. Ca B. Zn C. Al D. Mg
Đọc tiếp
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là
A. Ca
B. Zn
C. Al
D. Mg
Đáp án C
Các phương trình phản ứng :
M tác dụng với O2: 4 M + 2 n O 2 → t 0 2 M n O n
Chất rắn sau phản ứng tác dụng với dung dịch HCl thu được khí H2, chứng tỏ chất rắn sau có M dư nên O2 hết - chất rắn sau gồm M dư và M2On :
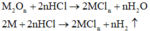
Tính toán:
Số mol H2 thu được là: n H 2 = 13 , 44 22 , 4 = 0 , 6 m o l
Sơ đồ phản ứng:
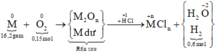
Các quá trình nhường, nhận electron cho cả quá trình:
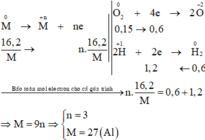
Đúng 0
Bình luận (0)
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100ml dung dịch A (d 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là: A. C3H8O2 B. C7H8 C. C4H8O3 D. C6H6.
Đọc tiếp
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100ml dung dịch A (d = 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là:
A. C3H8O2
B. C7H8
C. C4H8O3
D. C6H6.